
AEMPS ha informat sobre la retirada d'alguns dispositius de autoinyección d'adrenalina del medicament EMERADE a causa d'un possible defecte de qualitat. Es tracta d'un medicament clau per a persones amb el risc de patir reaccions al·lèrgiques severes (aliments, picades d'insectes, etc.).
Pharmaswiss Ceska Republika, S.RO, empresa comercialitzadora de EMERADE, ha informat l'Agència Espanyola de Medicaments i Productes Sanitaris (AEMPS) d'un possible defecte de qualitat en el dispositiu de *autoinyección. Això provoca que algunes unitats calga forçar-les per a activar l'administració de la dosi. Com a conseqüència d'això, existeix el risc que no s'administre la dosi requerida, suposant un risc potencial per a la vida del pacient.
Aquest problema no està associat a lots concrets, per la qual cosa podria aparéixer en qualsevol ploma d'aquest medicament. Els medicaments afectats són:
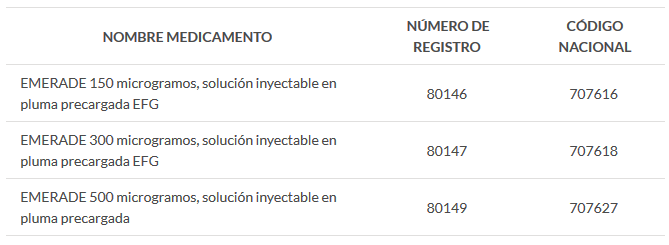
Com a conseqüència d'això, AEMPS ha ordenat la retirada de totes les unitats de EMERADE presents en el canal de distribució, farmàcies i en possessió dels pacients.
Així mateix, i amb la intenció que els usuaris disposen de medicaments sense aquest defecte potencial, es procedirà a la seua substitució per altres dispositius d'adrenalina alternatius, de manera totalment gratuïta:
AEMPS ha demanat als laboratoris fabricadors dels medicaments alternatius que incrementen les unitats posades en el mercat perquè les substitucions necessàries es duguen a terme al més prompte possible. No obstant això, l'Agència ha advertit que existeix la possibilitat que aquest augment en la demanda per a substituir les unitats defectuoses de *EMERADE comporte problemes de subministrament puntuals.
Recomanacions AEMPS
En últim lloc, AEMPS ha establit certes indicacions per als pacients al·lèrgics que segueixen un tractament a base d'adrenalina EMERADE:
Consulta la notícia original AQUI